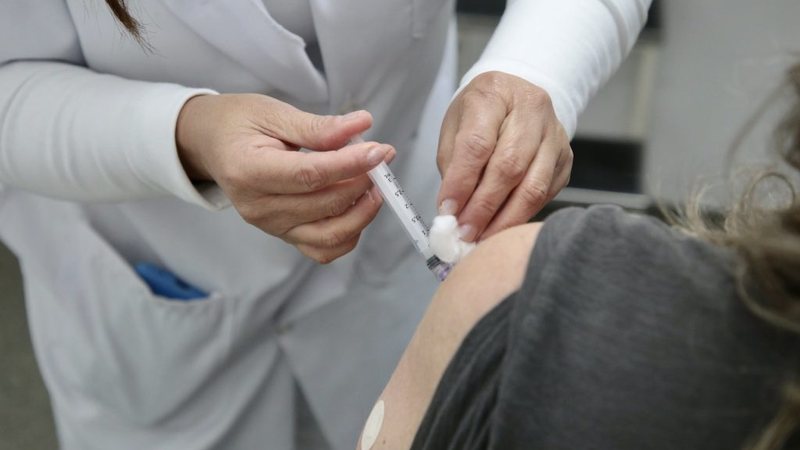
Canetas emagrecedoras manipuladas abrem debate sobre qualidade e riscos
Freepik

São Paulo -A Agência Nacional de Vigilância Sanitária (Anvisa) discute nesta quarta-feira, 29, a Proposta de Instrução Normativa (IN) para estabelecer os requisitos técnicos para importação, qualificação de fornecedores e controle de qualidade aplicáveis à manipulação de agonistas de GLP-1 - conhecidas como canetas emagrecedoras.
Leia também: Anvisa vai discutir normas para manipulação de canetas emagrecedoras
A nova norma faz parte de um conjunto de estratégias incluído no plano de ação, anunciado em 6 de abril, que prevê medidas regulatórias e de fiscalização relacionadas a esses produtos.
Hoje, a manipulação desses medicamentos tem autorização para que o composto seja manipulado e vendido por farmácias magistradas em casos específicos, que buscam atender a determinado paciente que não se adapta às doses disponibilizadas pela indústria, por exemplo.
Riscos
Apesar de considerar a IN um avanço para a segurança na produção desses medicamentos, o diretor da Sociedade Brasileira de Endocrinologia e Metabologia (SBEM) Clayton Macedo avalia que a IN não irá suprir as brechas ainda presentes nas regras de manipulação, tendo em vista que, enquanto elas existirem, nenhuma estrutura de fiscalização dará conta de combater a alta demanda e a produção desenfreada.
O objetivo da farmácia de manipulação é customizar uma prescrição individual. Então, o médico atende o paciente, aquele paciente precisa da medicação em uma dose que não tem no mercado. Ela é para para uso excepcional e não é para uso do jeito que está sendo feito, no qual as farmácias se transformam em indústrias sem o rigor técnico da indústria."
Ele ressalta que as canetas originais desses medicamentos, como a semaglutida e a tirzepatida, já permitem a titulação e o ajuste de doses para minimizar efeitos adversos, o que derruba a justificativa técnica para a produção manipulada, que pode ser feita de forma massiva por farmácias, fugindo do princípio da manipulação.
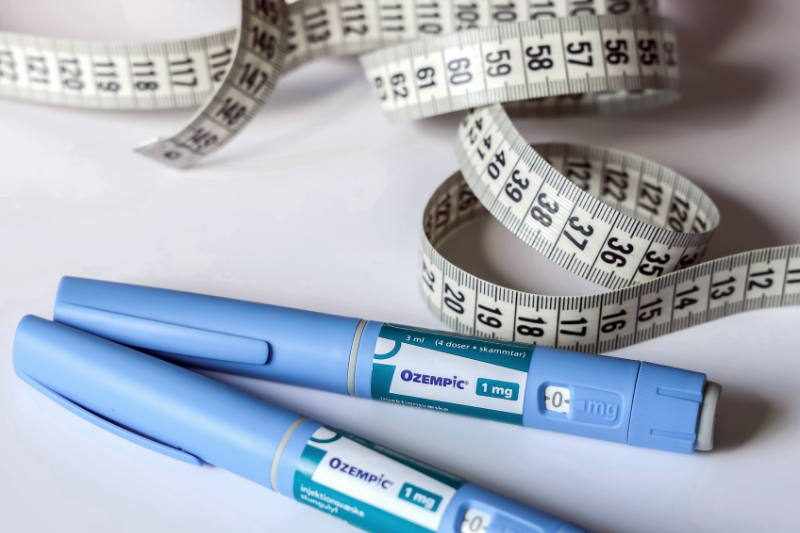
A Eli Lilly, fabricante do Mounjaro (tirzepatida), tem uma posição semelhante à de Macedo. A empresa destaca que entende que os requerimentos da IN, apesar de importantes, são insuficientes para a real proteção dos pacientes.
"É inegável que a IN eleva o padrão exigido em relação à normativa atual. Porém, a Lilly entende que os requerimentos são insuficientes para a real proteção dos pacientes – e, mantidos como estão, podem produzir efeito inverso: conferir aparência de legitimidade a produtos que, na prática, não têm segurança, qualidade e eficácia asseguradas", atesta a empresa.
A marca leva em conta também a complexidade biológica desses elementos, principalmente a tirzepatida. "Independentemente da rota de produção, é uma macromolécula de estrutura complexa, com perfil de risco mais próximo ao dos produtos biológicos do que ao das pequenas moléculas sintéticas convencionais", afirma
Sobre a forma como a manipulação vem ocorrendo na prática, as fontes destacam graves problemas:
Produção industrial sem rigor técnico
O diretor da SBEM destaca que farmácias de manipulação estão operando como indústrias, realizando produção em série e formando estoques, mas sem o rigor e as boas práticas da indústria farmacêutica.
Esses produtos raramente são vendidos nos balcões; eles são enviados diretamente para clínicas que vendem "protocolos" de emagrecimento ou até mesmo podem ser contrabandeados de outras regiões e vendidos sem prescrição médica.
A fabricante do Mounjaro também destaca que a IN não enfrenta a produção em lote feita antes mesmo de haver uma prescrição individualizada (formação de estoque).
Ausência de testes e bioequivalência
Os sais que servem como matéria-prima desses tipos de medicamentos vêm de locais como Índia e China e não são divulgados para o mercado.
Leia também: Canetas emagrecedoras 'piratas' são proibidas pela Anvisa; saiba motivo
"Por se tratarem de moléculas extremamente complexas, como a tirzepatida, que se liga a dois receptores, é impossível garantir que a estrutura espacial do manipulado seja a mesma da molécula original, o que significa que não há comprovação de sua bioatividade, segurança ou eficácia clínica", destaca Macedo.
Riscos de reações e intoxicação
Moléculas manipuladas inadequadamente podem formar compostos imunogênicos que geram reações alérgicas desconhecidas. Ele cita dados do FDA, dos Estados Unidos, demonstrando que a liberação temporária desses manipulados resultou em um grande aumento de casos de intoxicação, com amostras apresentando baixíssima pureza e sobredoses de até 38,8% acima do indicado.
Erros de aplicação e conservação
Para Macedo, a margem de erro é altíssima na hora de administrar a medicação, pois muitas vezes é necessário converter a dose em miligramas para unidades em seringas de insulina, levando pacientes a superdosagens graves e até internações. .
Além disso, há incertezas sobre a esterilidade dos produtos e falhas na conservação térmica, uma vez que toda a cadeia de transporte precisa ser rigorosamente refrigerada.
Testar o IFA não garante segurança do produto final
A Lilly argumenta que exigir a caracterização analítica Insumo Farmacêutico Ativo (IFA) - substância que dá ao medicamento a sua característica farmacêutica, que faz determinado medicamento funcionar - como pureza e sequência de aminoácidos e a certificação CADIFA do processo de fabricação é insuficiente.
A empresa destaca que aprovar o insumo nesses testes não significa que o produto final manipulado terá a mesma eficácia e segurança do medicamento original, pois a estrutura tridimensional e a potência podem ser totalmente diferentes.
Paciente não é levado em conta
Para o diretor da SBEM, no atual cenário de manipulados para emagrecimento, o paciente não é o foco principal de cuidado, mas sim alvo de um modelo de negócios altamente lucrativo, que o expõe a diversos riscos.
"Esse mercado não atinge a população carente hoje e não baixou o preço em lugares como os EUA e não foi vendido para população carente. Então esses movimentos são na realidade um escudo para que as empresas sigam produzindo para esse mercado que eles mesmos chamam de 'high ticket' (ticket alto)", explica.
Ele acrescenta ainda que, quando os pacientes sofrem efeitos adversos sérios provenientes de uma manipulação mal feita como náusea e gastrite, eles raramente denunciam.
O endocrinologista explica que as pessoas se sentem envergonhadas por terem caído nessa rede de extorsão financeira, o que inviabiliza a farmacovigilância no Brasil e impacta a avaliação do verdadeiro impacto da manipulação desenfreada desses produtos.
Em nota a SBEM a sugere e recomenda a proibição da manipulação desses fármacos, como medida mais efetiva para reduzir risco e proteger a população.
"É necessário reconhecer que estamos diante de fármacos de alta complexidade biológica, cujo comportamento clínico não pode ser inferido apenas por testes laboratoriais pontuais", alerta a entidade.
Leia também: Anvisa vai endurecer fiscalização de manipulação de canetas emagrecedoras
A sociedade destaca que em peptídeos dessa natureza, pequenas variações no processo produtivo ou na composição final podem resultar em alterações relevantes de eficácia, segurança e imunogenicidade.
O risco para o paciente não decorre apenas da identidade química da molécula principal, mas do conjunto de variáveis envolvidas, incluindo impurezas e agregação molecular.
Duas medidas
O diretor da SBEM avalia que a Anvisa tem sido muito rígida ao analisar pedidos de registro de novas versões de canetas similares da semaglutida e da liraglutida- cujas patentes já caíram.
"A agência chegou a negar vários processos de registro industrial por considerar os dados insuficientes, reconhecendo a enorme complexidade dessas moléculas. No entanto, através da IN, a Anvisa estaria aceitando um padrão muito inferior", avalia.
Ele destaca que o padrão aprovado ainda é diferente para o mesmo princípio ativo quando ele é manipulado, não exigindo dados de eficácia clínica e ignorando que a manipulação possui controles estruturalmente muito menores que a indústria atualmente.
Comentários
Política de comentários
Este espaço visa ampliar o debate sobre o assunto abordado na notícia, democrática e respeitosamente. Não são aceitos comentários anônimos nem que firam leis e princípios éticos e morais ou que promovam atividades ilícitas ou criminosas. Assim, comentários caluniosos, difamatórios, preconceituosos, ofensivos, agressivos, que usam palavras de baixo calão, incitam a violência, exprimam discurso de ódio ou contenham links são sumariamente deletados.